O aproveitamento de resíduos florestais vem se tornando cada dia mais atrativo, pois eles são uma fonte renovável de energia. A figura representa a queima de um bio-óleo extraído do resíduo de madeira, sendo ΔH1 a variação de entalpia devido à queima de 1g desse bio-óleo, resultando em gás-carbônico e água líquida, e ΔH2 a variação de entalpia envolvida na conversão de 1g de água no estado gasoso para o estado líquido.
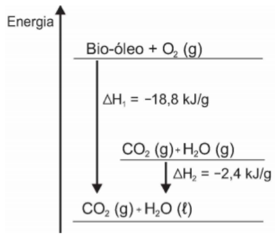
A variação de entalpia em kJ, para a queima de 5g desse bio-óleo resultando em CO2 (gasoso) e H2O (gasoso) é:
a) -106.
b) -94,0.
c) -82,0.
d) -21,2.
e) -16,4
Resposta
A entalpia liberada na queima é H = -18,8 kJ/g – (-2,4 kJ/g) = 16,4
Isso significa que são liberados 16,4 kJ por grama de g bio-óleo.
Podemos fazer uma regra de 3:
16,4 kJ – 1 g bio-óleo
x – 5 g bio-óleo
x = 5 . 16,4 = 82
Logo H = -82 kJ.
Letra C
