Eletroquímica (dia 25/agosto/2015)
A eletroquímica estuda o aproveitamento do fenômeno da transferência de elétrons entre átomos.
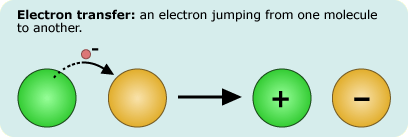
Essa transferência de elétrons pode gerar ou consumir energia, dependendo do sentido da reação.
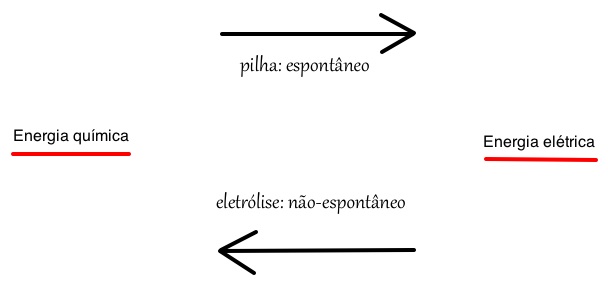
PILHA: A conversão de energia química em energia elétrica é um processo espontâneo chamado de de pilha ou de célula galvânica.

ELETRÓLISE: A conversão de energia elétrica em energia química é um processo não-espontâneo, chamado de eletrólise.

Veja o esquema explicativo:
Introdução
As reações de redução e oxidação envolvem a transferência de elétrons entre as substâncias. Essas reações acontecem simultaneamente, porque se um átomo ganha um elétron é porque outro perdeu.
Aqui você vai entender:
- porque aquele seu anel ficou preto. (Ele sofre oxidação).
- como as fotografias são reveladas (ENEM 2014).
- Como as pilhas funcionam
É importante se familiarizar com os conceitos principais de óxido-redução.
O átomo ou íon que doa elétrons, logo sofre oxidação, é chamado de redutor (ou agente redutor) porque provoca o ganho de elétrons (redução) de outro átomo ou íon.
Similarmente,
O átomo ou íon que ganha elétrons, logo sofre redução, é chamado de oxidante (ou agente oxidante) porque provoca a perda de elétrons (oxidação) de outro átomo ou íon.
De maneira mais explicativa, vejamos o caso do anel de prata:
A oxidação é a perda de elétrons.
Então, por exemplo, se seu anel de prata Ag foi oxidado, ele perdeu elétrons, e se tornou Ag+1.
Esta é a meia reação de oxidação: Ag -> Ag+1 + 1e-
Bom, o elétron da prata precisa ir para algum lugar. Ele irá para o oxigênio que sofrerá redução.
Esta é a meia reação de redução: O2 + 4e- -> 2O2-
Reação global: 4Ag +O2 -> Ag2O
Portanto:
Na oxidação o NOX aumenta, 0 para +1: Ag para Ag+1
Na redução o NOX diminui, 0 para -2: O0 para O2-
A prata sofreu oxidação, então ela causou a redução do oxigênio, assim, a prata é o agente redutor.
Quem sofre oxidação é o agente redutor.
O oxigênio sofreu oxidação, então ele causou a oxidação da prata, assim, o oxigênio é o agente oxidante.
Quem sofre redução é o agente oxidante.
Lembre sempre que quem sofre oxidação é o agente redutor e quem sofre redução é o agente oxidante. Sempre o contrário, ok?

